Publicidade:
Jogue Tibia sem mensalidades!
Taleon Online - Otserv apoiado pelo TibiaBR.
https://taleon.online
 Curtir: 0
Curtir: 0
num prisma regular de base quadrada a aresta da base é a metade da aresta lateral. se a area lateral é de 128 , qual é a sua area total?
o resultado tem que dar 160, meu resultado nunca chega nisso
alguem ai ajuda e explica como chega nesse resultado pls
Área de cada lado = 128/4 = 32
Area do lado = B*A = Aresta * Aresta/2 = Aresta² / 2
Aresta²/2 = 32
Aresta = 8
Aresta da base = 4
Área da base = 16
Área da base + área da parte de cima + área lateral = 16 + 16 + 128 = 160
Vc deve ta se confundindo pq deve ta fazendo a área lateral como um quadrado, mas é um retângulo (faça o desenho começando pela base e vai entender).
Edit: Uma figura pra vc entender
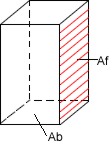
Última edição por Sete; 12-05-2011 às 17:55.
Ler livros e jornais não vai ensinar o que é objeto direto e indireto e verbos de ligação, etc e tudo mais.
Essa matéria é meio chata, até eu acho, mas para estudar tem que fazer exercícios, não tem outro jeito. O que exatamente você está estudando? Talvez eu possa ajudar, mas essas áreas eu ainda não conheço muito em português.
Uma pergunta sobre homossexualismo. A pessoa nasce gay? É algo que ela não tem controle de escolher? O modo de criação da criança pode alterar algo?
Gostaria de provas.
.
Última edição por luizjuiz; 04-07-2015 às 13:51.
Separando os 3 tópicos da sua pergunta:
A pessoa nasce gay?
Segundo a Super, de 15 a 25% dos gays desenvolvem a sexualidade dentro do útero.
Postado originalmente por Superinteressante, Jan-2011
Criação? Fui criado na ausência de um referencial de masculinidade (filho de mae solteira, até os 11~12 anos só brincava de casinha com as primas) e mesmo assim sou hetero.
A pessoa tem o controle de decidir? Acho que não, mas isso não tenho como provar, a não ser usando a lógica. Aposto que se fosse dado o direito de escolha, muitos gays escolheriam não ser gays, devido ao imenso preconceito que ainda sofrem (ainda hoje ha caras sendo expulsos de casa por serem gayspeguem como exemplo familias rigidas/religiosas).
Alias, essa é uma pergunta que carrega certo preconceito embutido, mas enfim. Voce se sente atraido por um belo decote, certo? Por que um peito forte e cabeludo não te atrai. Tente se sentir atraido por um homem. É bem provavel que não consiga. O prazer é um dos sentimentos mais complexos da espécie humana, e não falo apenas de prazer sexual. Por que voce gosta de (sente prazer com) tibia e não gosta de... Logaritmos (na boa, NINGUEM gosta de logaritmos). Isso é algo muito irracional, vai além do direito de escolha. E aquela historia do "vai indo aprende a gostar"? Nao vale a pena nem ser citada aqui, seria uma situação irreal demais.
Valar Morghulis
Seguinte, não é uma pergunta e sim um pedido, predão a abusadez
Eu estou viajando, logo ñ levei livros para estudos, mas necessito de livros de física, visto que a UERJ já está quase em cima e nada sei sobre física.
Qualquer PDF e cias com explicações/exercicios seria MUITO BEM vindo
Principalmente de eletricidade, visto que ñ consigo estudar pela wikipedia.
Muitos beijos e dinheiros a quem me responder
Ps: Postar nome de bons livros/apostilas tb seria uma contribuição bem vinda.
Última edição por Daniel Passy; 17-05-2011 às 13:29.
usuário random nº 1
Bom pessoal, estou com dificuldade em alguns problemas de Quimica, na parte de Gases. Alguem que entende dessa parte poderia fazê-los passo a passo, por favor? :triste:
(fuvest) Certo refrigerante é engarrafado, saturado com dióxido de carbono (CO2) a 5ºC e 1 atm de CO2 e então fechado. Um litro desse refrigerante foi mantido algum tempo em ambiente à temperatura de 30ºC. Em seguida, a garrafa foi aberta ao ar (pressão atmosférica = 1 atm) e agitada até praticamente todo o CO2 sair. Nessas condiçoes (30ºC e 1 atm), qual o volume aproximado de CO2 liberado?
DADOS:
Massa molar do CO2 = 44 g/mol
Volume molar dos gases a 1 atm e 30ºC = 25 L/mol
Solubilidade do CO2 no refrigerante a 5ºC e sob 1 atm de CO2 = 3,0 g/L
a) 0,40L
b) 0,85L
c) 1,7L
d) 3,0L
e) 4,0L
(fuvest) Têm-se três cilindros de volumes iguais e à mesma temperatura, com diferentes gase. Um deles contém 1,3kg de acetileno (C2H2); o outro, 1,6kg de óxido de dinitrogênio (N2O); e o terceiro, 1,6kg de oxigênio (O2). Comparando-se as pressões dos gases nesses três cilindros, verifica-se que:
MASSAS MOLARES (g/mol)
C2H2 = 26
N2O = 44
O2 = 32
a) são iguais apenas nos cilindros que contêm N2O e O2
b) são iguais apenas nos cilindros que contêm C2H2 e O2
c) são iguais nos três cilindros
d) é maior no cilindro que contêm N2O
e) é menor no clindro que contêm C2H2
(UFRGS-RS) Dois recipientes idênticos, mantidos na mesma temperatura, contêm o mesmo número de moléculas gasosas. Um dos recipientes contém hidrogênio, enquanto o outro hélio. Qual das afirmações abaixo está correta? (H=1; He=4)
a) A massa de gás em ambos os recipientes é idêntica.
b) A pressão é a mesma nos dois recipientes.
c) Ambos os recipientes contêm o mesmo número de átomos.
d) A massa gasosa no recipiente que contém hidrogênio é o dobro da massa gasosa no recipiente que contém hélio.
e) A pressão no recipiente que contém hélio é o dobro da pressão no recipiente que contém hidrogênio.
(UFRGS-RS) Dois recipientes A e B, de paredes rígidas, apresentam iguais volumes. O recipiente A contém uma massa de hélio (he) igual à massa de metano (CH4) contida no recipiente B. Inicialmente os dois gases estão a 100K. Elevando-se a temperatura do metano para 400K, sua pressão em relação ao hélio será, aproximadamente: (H=1; He=4; C=12)
a) quatro vezes menor
b) a metade
c) a mesma
d) o dobro
e) quatro vezes maior
(UNESP) Sabendo-se que o volume molar de um gás nas condições normais de temperatura e pressão (CNTP) é igual a 22,4L e que R= 0,082, o maior número de moléculas está contido em 1,0L de:
a) H2, nas CNTP
b) N2, nas CNTP
c) H2, a -73ºC e 2 atm
d) H2, a 27ºC e 1 atm
uma mistura equimolar de H2 e N2, a 127ºC e 1,5 atm
(UFF-RJ/2000) Tem-se uma amostra gasosa formada por um dos seguintes compostos:
CH4; C2H4; C2H6; C3H6 ou C3H8
Se 22g dessa amostra ocupam o volume de 24,6L à pressão de 0,5 atm e temperatura de 27ºC (dado R= 0,082), conclui-se que se trata do gás: (C=12; H=1)
a) etano
b) metano
c) propano
d) propeno
e) eteno
Informação: etano (C2H6), metano (CH4), propano (C3H8), propeno (C3H6) e eteno (C2H4)
Gabarito é : c, b, b, c, c, c.